Die Konferenzen
Die Aseptik-Konferenz und die Mikrobiologie-Konferenz sind seit vielen Jahren feste Bestandteile der deutschsprachigen Konferenzlandschaft der pharmazeutischen Industrie.
Vor fünfzehn Jahren wurde der Kongress „aseptikon“ ins Leben gerufen, der die Themengebiete aseptische Herstellung, Mikrobiologie und zugehörige aktuelle Themen zusammenfasst.
Zusätzlich bietet die angeschlossene Fachausstellung rund um Mikrobiologie, Hygiene und Reinraummonitoring Ausstellern die Möglichkeit, ihre Dienstleistungen und Produkte einem interessierten Publikum zu präsentieren.
In diesem Jahr beinhaltet die aseptikon die folgenden Veranstaltungen:
- 25. Deutsche Aseptik-Konferenz
- 16. Deutsche Mikrobiologie- und Hygienekonferenz
- Reinraum – Laufender Betrieb und Verbrauchsmaterialien
- Quality Oversight in der Sterilherstellung
- Technische Umsetzung des Annex 1
Die aseptikon im Überblick
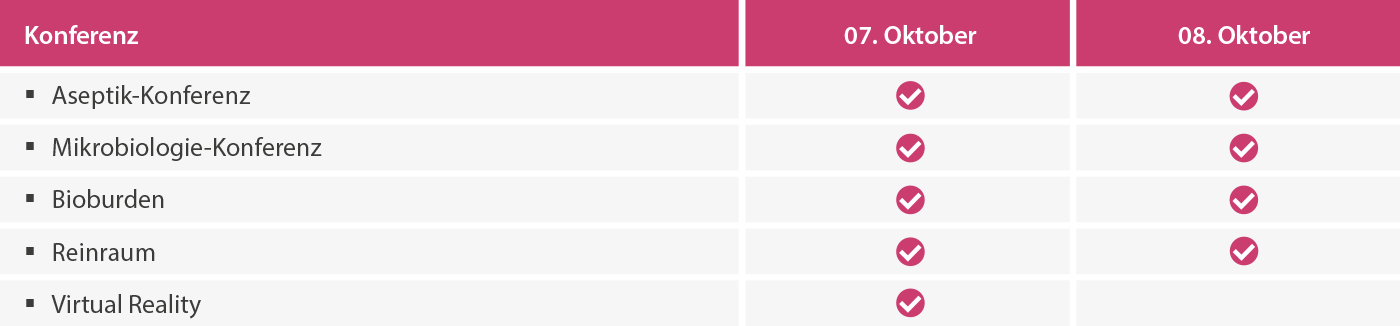
06./07. Oktober
Highlights
- Praxisnahe Umsetzung der Annex-1-Anforderungen bei Isolatoren, Sterilfiltration und Single-Use-Systemen
- Risikobasierter Umgang mit „Aging Facilities“ und Retrofit bestehender aseptischer Anlagen
- Mikrobiologische Kontaminationskontrolle und CCS-Strategien anhand realer Fallbeispiele
- Aktuelle behördliche Erwartungen und Interpretationen des Annex 1 – von Steriltest bis NTT-Prozess
- Herausforderungen und Lösungsansätze bei Desinfektion, Integritätstests und Barrieresystemen in der aseptischen Herstellung
Zielsetzung
Die aseptische Herstellung steriler Arzneimittel steht durch den revidierten EU GMP Annex 1 weiterhin vor großen technischen, mikrobiologischen und regulatorischen Herausforderungen. Ziel dieser Votragsreihe ist es, aktuelle Anforderungen des Annex 1 praxisnah zu beleuchten und konkrete Lösungsansätze für die Umsetzung im pharmazeutischen Alltag aufzuzeigen. Im Fokus stehen sowohl moderne Barrieresysteme und deren Integrität als auch Sterilfiltration, Single-Use-Systeme, Desinfektion sowie mikrobiologische Kontaminationskontrolle als Bestandteil einer ganzheitlichen Contamination Control Strategy (CCS).
Darüber hinaus werden Herausforderungen im Umgang mit Bestandsanlagen, Retrofit-Projekten und „Aging Facilities“ diskutiert. Anhand von Praxis- und Fallbeispielen erfahren die Teilnehmenden, wie regulatorische Erwartungen interpretiert, technische Risiken bewertet und nachhaltige, inspektionssichere Lösungen etabliert werden können. Die Veranstaltung bietet zudem Raum für den Austausch über behördliche Erwartungen, unterschiedliche Interpretationen des Annex 1 sowie aktuelle Branchenpraktiken. Ziel ist es, den Teilnehmenden Orientierung für die GMP-konforme Weiterentwicklung aseptischer Prozesse und Anlagen zu geben.
06./07. Oktober
Highlights
- Erwartungen des Inspektors
- Schnellmethoden – Primärvalidierung
- Auffälligkeiten im mikrobiologischen Monitoring
- Mikrobiologische Kontrolle von Wasser
- Isolatoren beim Steriltest
- ISO-Normen und ARMM für eine effektive Luftüberwachung – Geht das zusammen?
- Laborumbau im laufenden Betrieb – eine Erfahrungsstudie
Zielsetzung
Der diesjährige Konferenztrack gibt Ihnen über zwei Tage einen Einblick in aktuelle Entwicklungen in den mikrobiologischen Kontrolllabors, von neuen Methoden und Systemen bis hin zu Anforderungen aus Richtlinien und Arzneibüchern. Dabei werden nicht nur neue Systeme vorgestellt, sondern auch deren Pros, Cons und Validierungsansätze diskutiert. Sich ändernde Richtlinien in den Guidelines und Arzneibüchern wie z. B. ICH Q5 (R2), Ph. Eur. Chapter 2.6.41. und andere verlangen Beachtung und Umsetzung. Damit ergeben sich Konsequenzen für viele Bereiche der Mikrobiologie, etwa in der Qualitätssicherung und Qualitätskontrolle, bei der Virussicherheit, beim Umgebungsmonitoring, bei Bioburdenbestimmungen, bei der Prüfung auf Sterilität bis hin zum Test auf Endotoxine bzw. Pyrogene. Darüber hinaus werden Themen wie Laboroptimierung, Modernisierung und Umbau eine Rolle spielen. Die Mikrobiologie- und Hygienekonferenz der aseptikon 2026 beleuchtet aktuelle Entwicklungen, und Expert/innen aus der Industrie, von den Arzneibüchern und aus Auftragslabors zeigen diese auf und liefern Lösungsansätze aus der Praxis.
06./07. Oktober
Highlights
- Hot Topics und Erfahrungen aus der Inspektion
- Aktuelle Entwicklungen im Reinraummonitoring
- Personalhygiene: Erfahrungen einer Auditorin
- Reinigung und Desinfektion
- Von der Theorie zur Praxis: Anforderungen, Umsetzung und mikrobiologische Qualifizierung eines Reinraumbekleidungskonzeptes – Fallstudien von CNC bis steril
- Handschuhe und mehr – Verbrauchsmaterialien im Reinraum
Zielsetzung
Im vorliegenden Konferenztrack werden Ihnen zum einen die Erwartungen der Kontrollbehörden an die Reinräume im laufenden Betrieb vorgestellt,
zum anderen aber auch ein Einblick an die Anforderungen verwendeter Verbrauchsmaterialien gegeben. Ob einmal verwendbar oder
wiederverwendbar - erfahrene Referent/innen stellen Ihnen die Eigenschaften, Verwendbarkeit und auch Einschränkungen vor, die verschiedene
Verbrauchsgüter bzw. verwendete Materialien wie Kleidung, Tücher, Desinfektionsmittel etc. mit sich bringen und informieren über Anwendung
und Gebrauch im laufenden Betrieb.
07. Oktober
Highlights
- Erwartungen der FDA an die QA-Oversight
- Erwartungen aus Sicht eines GMP Inspektors
- QA-Oversight in Zeiten der digitalen Transformation
- Typische Probleme in der Praxis
- Fallstudien zu QA-Oversight unter anderem von
- Boehringer Ingelheim Pharma
- Vetter Pharma-Fertigung
- Loba biotech
Zielsetzung
Dieser Konferenztrack vermittelt Ihnen ein kompaktes, regulatorisch fundiertes Verständnis von Quality Oversight in der aseptischen Herstellung. Im Fokus stehen die aktuellen FDA-Erwartungen sowie die europäischen Anforderungen aus EU GMP Annex 1 und Annex 15. Erhalten Sie Klarheit darüber, ob Quality Oversight ausschließlich eine FDA-Forderung ist, welche Erwartungen europäische Inspektoren stellen und wie sich anhand mehrerer Case Studies eine wirksame Qualitätsüberwachung über den gesamten Validierungslebenszyklus praktisch implementieren lässt. Ziel ist es, regulatorische Anforderungen sicher einzuordnen, Inspektionsrisiken zu minimieren und Quality Oversight strategisch als Mehrwert für das eigene Unternehmen zu nutzen.
06. Oktober
Highlights
- Praxisnahe Umsetzung der Annex-1-Anforderungen in modernen Fill-&-Finish-Anlagen
- Retrofit bestehender Maschinen versus Neubau – technische Strategien im Vergleich
- Reduktion menschlicher Eingriffe durch neue Zuführsysteme, Automatisierung und Robotik
- Aktuelle Inspektionsschwerpunkte bei Sterilfiltration und Dampfsterilisation
- Erfahrungsberichte aus der aseptischen Produktion und Gefriertrocknung eines CMO
Zielsetzung
Dieser Track beleuchtet die technische Umsetzung zentraler Anforderungen aus EU GMP Annex 1 in der aseptischen Herstellung. Im Fokus stehen praxisnahe Lösungen für bestehende und neue Fill-&-Finish-Anlagen, Retrofit-Strategien, moderne Zuführsysteme, Sterilfiltration, Dampfsterilisation sowie die Reduktion manueller Eingriffe durch Automatisierung und Robotik. Anhand konkreter Umsetzungs- und Inspektionsbeispiele wird gezeigt, wie regulatorische Erwartungen in belastbare technische Maßnahmen übersetzt werden können. Die Teilnehmenden erhalten Orientierung für Investitionsentscheidungen, Modernisierungsprojekte und die GMP-konforme Weiterentwicklung aseptischer Prozesse – bis hin zu speziellen Anwendungen wie der Gefriertrocknung beim CMO.


